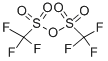
| Beschrijving |
Trifluormethaansulfonzuuranhydride, ook bekend als triflinezuuranhydride, heeft bewezen een buitengewoon reagens te zijn voor een breed scala aan transformaties. Als commercieel en gemakkelijk verkrijgbaar reagens wordt het op grote schaal gebruikt in de synthetische chemie vanwege zijn hoge elektrofiliciteit. Gezien zijn hoge affiniteit voor O-nucleofielen, wordt de reactie met alcoholen, carbonylen, zwavelfosfor- en jodiumoxides met betrekking tot de vorming van de overeenkomstige triflaten sterk begunstigd. Als een van de belangrijkste vertrekkende groepen in de organische chemie openen de gegenereerde triflaten vervolgens de deur naar verschillende stroomafwaartse transformaties, waaronder (maar niet beperkt tot) substitutiereacties, kruiskoppelingsprocessen, redoxreacties en herschikkingen[1-2] . |
| Chemische eigenschappen |
heldere kleurloze tot lichtbruine vloeistof |
| Toepassingen |
Trifluormethaansulfonzuuranhydride is een sterk elektrofiel dat wordt gebruikt bij de chemische synthese voor het introduceren van de triflylgroep. |
| Toepassingen |
Trifluormethaansulfonzuuranhydride wordt gebruikt om fenolen en imine om te zetten in triflic-ester en NTf-groep. Het is een sterke elektrofiel die wordt gebruikt voor de introductie van de triflylgroep in de chemische synthese. Het dient als reagens bij de bereiding van alkyl- en vinyltriflaten en voor de stereoselectieve synthese van mannosazidemethyluronaatdonoren. Het fungeert als katalysator voor glycosylatie met anomere hydroxysuikers om polysachariden te bereiden. |
| Definitie |
ChEBI: Triflinezuuranhydride is een organosulfonzuuranhydride. Het is functioneel verwant aan een triflinezuur. |
| Reactiviteitsprofiel |
Elektrofiele activering van tertiaire en secundaire amiden met triflinezuuranhydride (Tf2O; trifluormethaansulfonzuuranhydride) onder milde omstandigheden geeft aanleiding tot respectievelijk iminium- en iminotriflaten, die kunnen worden gebruikt als veelzijdige reagentia om te reageren met verschillende C-, N-, O- en S -nucleofielen voor de transformatie van een amidefunctie in verschillende producten. Andere zuurstofbevattende nucleofielen, zoals sulfoxiden en fosforoxiden, zouden ook een nucleofiele aanval met Tf2O kunnen ondergaan om thioniumtriflaat, elektrofiele P-soorten en fosfoniumtriflaat te genereren. Deze zeer actieve voorbijgaande soorten zouden gemakkelijk nucleofiele substitutiereacties kunnen ondergaan voor verdere diverse transformaties. Bovendien is Tf2O, vanwege de sterke elektrofiele eigenschap, geneigd te reageren met relatief zwakke nucleofielen zoals nitrilgroepen of sommige stikstofhoudende heterocyclische verbindingen. Bovendien is Tf2O ook gebruikt als een efficiënt radicaal trifluormethylerings- en trifluormethylthioleringsreagens door de afgifte van SO2 of deoxygenatieprocessen voor de synthese van trifluorgemethyleerde en trifluormethylthiolateerde verbindingen [2]. |
| Gevaar |
Kan bijtend zijn voor metalen. Schadelijk bij inslikking. Veroorzaakt ernstige brandwonden en oogletsel. |
| Ontvlambaarheid en explosiebaarheid |
Niet geclassificeerd |
| Synthese |
De synthese van trifluormethaansulfonzuuranhydride is als volgt:
Een droge rondbodemkolf van {{0}} ml wordt gevuld met 36,3 g. (0,242 mol) trifluormethaansulfonzuur (Opmerking 1) en 27,3 g. (0,192 mol) fosforpentoxide (Opmerking 2). De kolf wordt afgesloten en gedurende ten minste 3 uur bij kamertemperatuur bewaard. Gedurende deze periode verandert het reactiemengsel van een slurry in een vaste massa. De kolf is voorzien van een korte-wegdestillatiekop en wordt eerst verwarmd met een stroom hete lucht uit een warmtepistool en vervolgens met de vlam van een kleine brander.De kolf wordt verwarmd totdat er geen trifluormethaansulfonzuuranhydride meer destilleert, kookpunt 82–115 graden, wat 28,4–31,2 g oplevert. (83-91%) van het anhydride, een kleurloze vloeistof. Hoewel dit product voldoende zuiver is voor gebruik in de volgende stap, kan het resterende zuur door de volgende procedure uit het anhydride worden verwijderd. Een slurry van 3,2 g. fosforpentoxide in 31,2 g. van het ruwe anhydride wordt gedurende 18 uur bij kamertemperatuur in een afgesloten kolf geroerd. Nadat de reactiekolf is uitgerust met een korte-weg-destillatiekop, wordt deze verwarmd met een oliebad, wat 0,7 g oplevert. van de voorrun, bp 74-81 graad, gevolgd door 27,9 g. van het zuivere trifluormethaansulfonzuuranhydride, kookpunt 81-84 graden.

|
| opslag |
Opslaan in een koele, droge, goed geventileerde ruimte. Vochtgevoelig. |
| Zuiveringsmethoden |
Het kan vers worden bereid uit het watervrije zuur (11,5 g) en P2O5 (11,5 g, of de helft van dit gewicht) door het gedurende 1 uur bij kamertemperatuur te laten staan, de vluchtige producten af te destilleren en het vervolgens via een korte Vigreux-kolom te destilleren. Het wordt gemakkelijk gehydrolyseerd door H2O en ontleedt na een paar dagen aanzienlijk, waarbij SO2 vrijkomt en een stroperige vloeistof ontstaat. Bewaar het droog bij lage temperaturen. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referenties |
[1] Haoqi Zhang. "Trifluormethaansulfonzuuranhydride bij amideactivering: een krachtig hulpmiddel om heterocyclische kernen te smeden." TCIMAIL (2021).
[2] Dr. Qixue Qin, prof. dr. Ning Jiao, Zengrui Cheng. "Recente toepassingen van trifluormethaansulfonzuuranhydride bij organische synthese." Angewandte Chemie 135 10 (2022). |